Clascotérone et calvitie : mécanisme, études cliniques et statut en France (2026)
Le clascotérone (Winlevi), anti-androgène topique étudié contre l'alopécie : mécanisme, données Phase III et comparaison finastéride. Non autorisé pour la calvitie en France.

L'alopécie androgénétique touche près de 80 % des hommes au cours de leur vie et 40 % des femmes après la ménopause, selon l'OMS (2023). Pendant longtemps, l'arsenal thérapeutique s'est limité au minoxidil topique (1988) et au finastéride oral (1997) — ce dernier étant souvent abandonné en raison de ses effets secondaires sexuels (2-3 % des patients selon Kaufman et al., NEJM 1998). Le clascotérone, déjà commercialisé pour l'acné sous le nom Winlevi aux États-Unis (FDA 2020), est étudié comme une piste prometteuse : agir comme un anti-androgène, mais uniquement sur la peau où il est appliqué, sans absorption systémique significative.
Cette page fait le point, de façon strictement informative, sur ce que la recherche sait du clascotérone : mécanisme moléculaire, données cliniques Phase III, profil de sécurité comparé au finastéride, posologie évaluée dans les essais, et statut réglementaire en France.
Le clascotérone ne dispose d'aucune autorisation de mise sur le marché (AMM) en France ni en Europe pour l'alopécie à ce jour (mise sur le marché estimée entre 2027 et 2028, sous réserve des essais en cours). La seule forme autorisée est le Winlevi 1 % indiqué pour l'acné aux États-Unis (FDA 2020). Cette page est un contenu d'information scientifique : Renaissance Clinique est une clinique de greffe de cheveux et ne prescrit ni ne délivre ce médicament. Pour tout traitement médicamenteux, l'avis d'un médecin (dermatologue) est indispensable.
Qu'est-ce que le clascotérone ?
Le clascotérone (DCI : clascoterone, code de développement CB-03-01, nom chimique cortexolone 17α-propionate) est une petite molécule appartenant à la famille des stéroïdes 17α-propanoate. Sa structure ressemble à celle de la dihydrotestostérone (DHT), mais elle possède une particularité essentielle : elle se métabolise rapidement en cortexolone, un dérivé inactif, dès qu'elle pénètre dans la circulation sanguine. Sa demi-vie systémique est inférieure à 5 minutes.
Cette caractéristique pharmacocinétique confère au clascotérone son profil d'efficacité locale uniquement : la molécule bloque les récepteurs androgéniques au niveau du follicule pileux mais n'a quasiment aucun impact systémique. Selon la notice FDA Winlevi (2020), aucune variation significative des taux plasmatiques de testostérone, DHT, cortisol ou ACTH n'a été observée même à des doses 10 fois supérieures à la dose thérapeutique.
Mécanisme d'action au niveau du follicule pileux
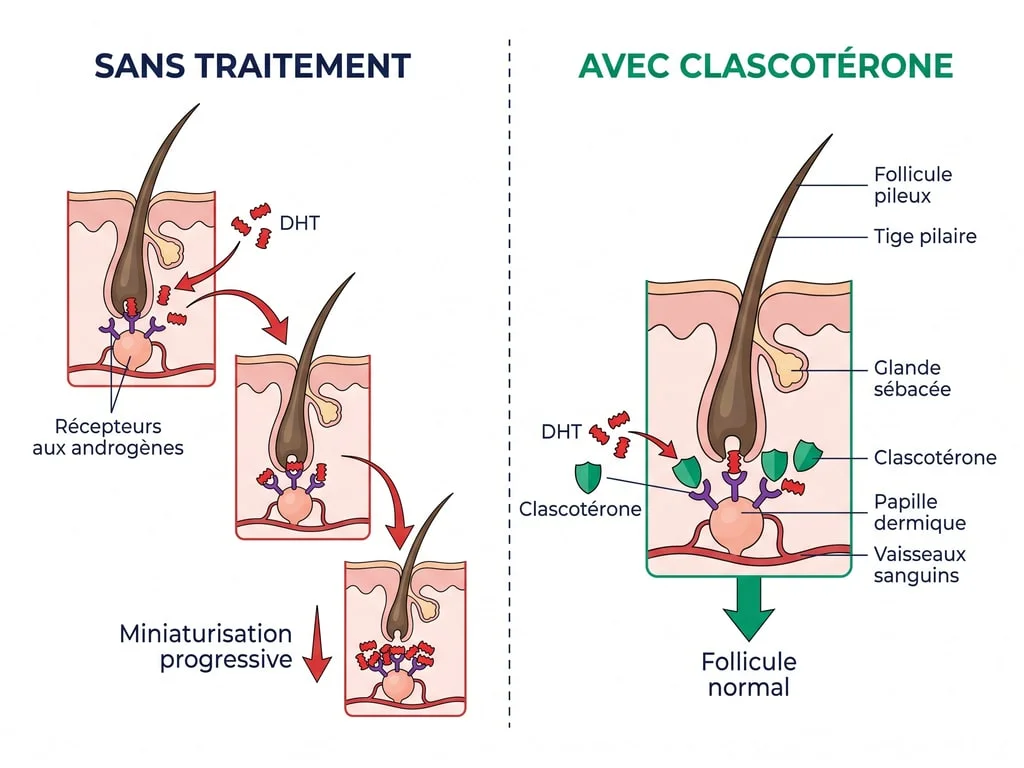
Dans l'alopécie androgénétique, la DHT (dihydrotestostérone) se lie aux récepteurs androgéniques présents sur les cellules de la papille dermique du follicule. Cette liaison déclenche une cascade de signalisation qui entraîne la miniaturisation progressive du follicule : les cheveux deviennent de plus en plus fins, puis ne repoussent plus.
Le clascotérone agit comme un antagoniste compétitif du récepteur aux androgènes : il occupe le site de liaison sans déclencher la cascade. Contrairement au finastéride qui inhibe l'enzyme 5α-réductase et donc la production systémique de DHT (réduction de 65-70 % selon Kaufman 1998), le clascotérone laisse les taux sanguins de DHT inchangés tout en protégeant le follicule.
Données cliniques Phase III (Breezula 7,5 %)
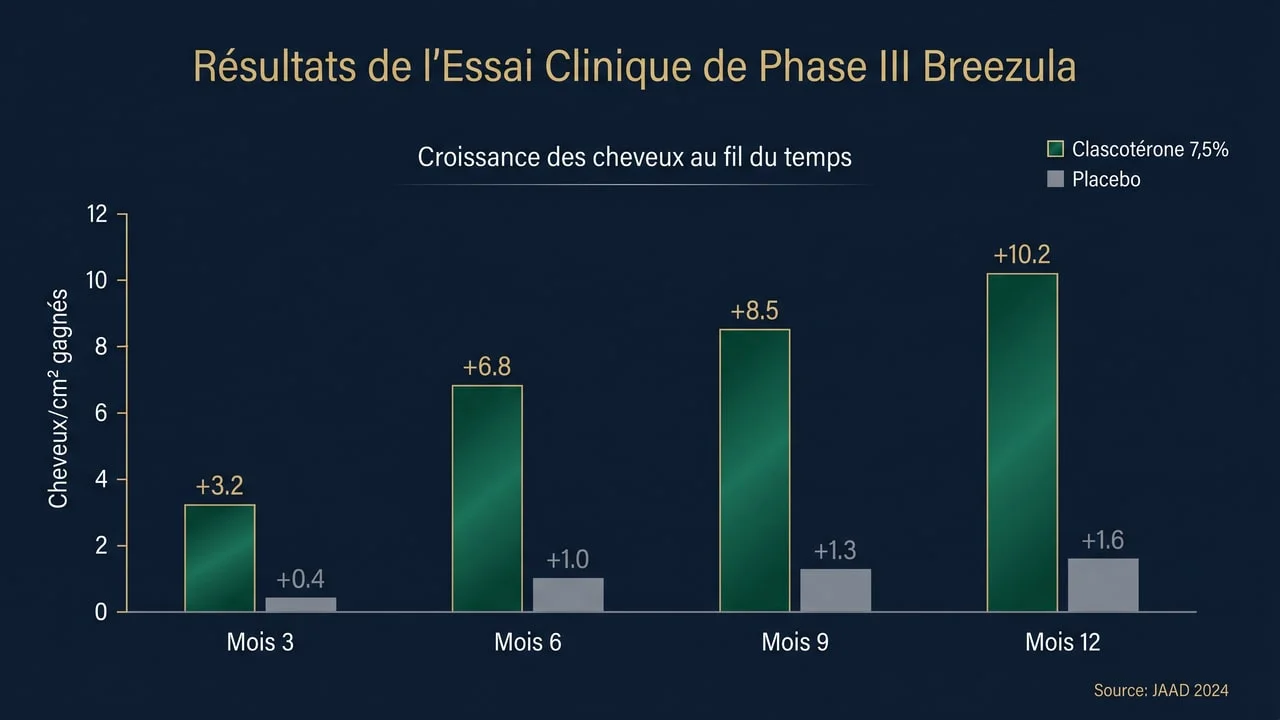
Les essais Breezula menés par Cassiopea (devenue Cosmo Pharmaceuticals) ont évalué une formulation topique à 7,5 % chez des hommes de 18 à 55 ans atteints d'alopécie androgénétique de stade III à IV (Hamilton-Norwood). Selon Piraccini et al. (JAAD 2024), les résultats à 12 mois sur 504 patients randomisés montrent :
Le pic d'efficacité est observé entre M6 et M12. Selon Cosmo Pharmaceuticals (communiqué Phase III, 2024), 73 % des patients ayant complété les 12 mois ont choisi de poursuivre le traitement en open-label extension — un indicateur fort d'acceptabilité réelle.
Études Phase II antérieures et historique de développement
Le développement clinique du clascotérone pour l'alopécie a commencé en 2014 avec les premières études Phase II menées par Cassiopea (Italie). Trichoster TR-13/14 (Phase II, n=210 hommes, formulation 1 % et 5 %) a établi la dose-réponse et orienté Phase III vers la concentration 7,5 %. Une seconde étude Phase II a inclus 96 femmes pré-ménopausées atteintes d'alopécie androgénétique féminine (FPHL) — résultats préliminaires positifs (publication en cours).
La forme à 1 % (Winlevi) a obtenu son AMM FDA en août 2020 pour l'acné modérée à sévère, ce qui constitue la base réglementaire de la molécule. La concentration 7,5 % spécifique à l'alopécie est en cours d'évaluation FDA et EMA, avec une mise sur le marché européen attendue entre 2027 et 2028 (sous réserve d'aboutissement des essais Phase III complémentaires).
Posologie et application pratique
Selon le protocole utilisé en Phase III Breezula, la posologie recommandée du clascotérone topique 7,5 % est :
- Fréquence : 2 applications par jour (matin et soir)
- Quantité : 1 ml par application (≈ 30 gouttes via pipette doseuse)
- Zone d'application : Cuir chevelu sec, zones de calvitie active (frontale, vertex, couronne)
- Méthode : Massage léger 30 secondes, sans rinçage
- Délai d'évaluation : 6 mois minimum, optimal 12 mois
L'application peut se faire avant ou après le shampoing, mais sur cheveux secs (l'eau dilue la pénétration). Selon la notice FDA Winlevi, il faut éviter le contact avec les yeux, les muqueuses, et se laver les mains après application.
Le clascotérone topique ne doit pas être appliqué sur des zones de peau lésée (psoriasis sévère, dermatite séborrhéique active, plaies). En post-greffe, attendre la cicatrisation complète (minimum 3 semaines après l'intervention FUE/Choi Pen). Selon les recommandations ISHRS (2024), l'introduction se fait à partir du M3 post-opératoire.
Comparaison avec le finastéride et le minoxidil
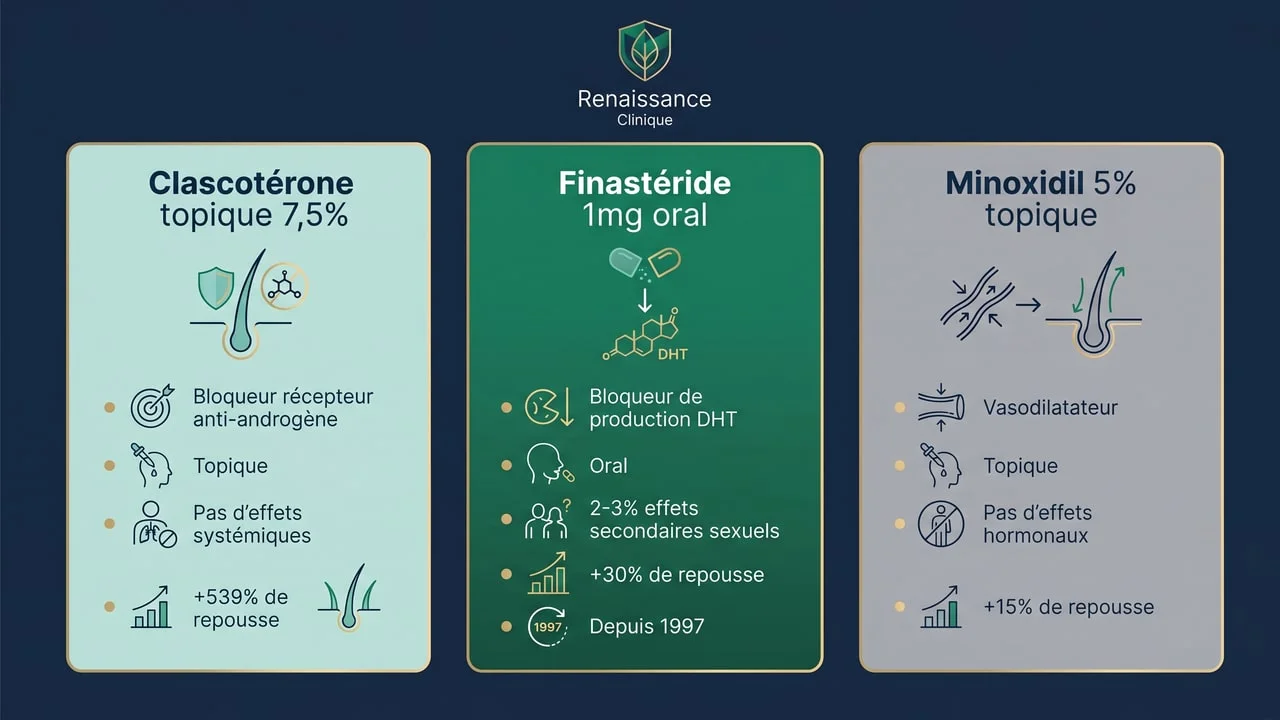
Deux traitements sont actuellement autorisés en France pour l'alopécie androgénétique masculine (finastéride, minoxidil) ; le clascotérone est une troisième molécule, encore en développement pour cette indication. Leurs profils sont complémentaires plus que concurrents :
| Critère | Clascotérone 7,5 % | Finastéride 1 mg | Minoxidil 5 % |
|---|---|---|---|
| Mécanisme | Bloque récepteur AR | Inhibe 5α-réductase | Vasodilatateur K+ channel |
| Voie d'administration | Topique 2x/j | Oral 1x/j | Topique 2x/j |
| Action systémique | Aucune | Oui (-65 % DHT) | Aucune |
| Effets sexuels | 0 % | 2-3 % | 0 % |
| Gain à 12 mois | +10,2 cheveux/cm² | +30 % de cheveux | +15 % de cheveux |
| Femme en âge de procréer | Compatible | Contre-indiqué | Compatible |
| Disponibilité France (2026) | Non commercialisé pour l'alopécie | 30-60 € / mois | 20-40 € / mois |
| AMM française | En attente (2027-2028 attendue) | Oui depuis 1997 | Oui depuis 1988 |
Selon l'ISHRS (Position Statement 2024), ces molécules peuvent être associées pour les cas réfractaires ou très évolutifs (association parfois appelée « trithérapie capillaire »). Une telle association relève d'une décision et d'un suivi médical individualisés, et suppose que chaque molécule soit disponible et prescrite par un médecin.
Profil de sécurité et effets secondaires
Le profil de tolérance du clascotérone est l'un de ses arguments majeurs. Les effets indésirables rapportés en Phase III (Piraccini, JAAD 2024) sont presque exclusivement locaux :
- Irritation cutanée légère : 5-8 % des patients (souvent transitoire, 2-4 premières semaines)
- Sécheresse du cuir chevelu : 3-5 %
- Prurit (démangeaisons) : 2-3 %
- Érythème transitoire : 1-2 %
Aucun signal hormonal systémique n'a été détecté dans les essais Phase III : libido, fonction érectile, taux de testostérone et de DHT plasmatiques restent inchangés. Cette caractéristique rend le clascotérone particulièrement attractif pour les patients ayant arrêté le finastéride en raison d'effets secondaires sexuels — y compris les rares cas de post-finasteride syndrome (PFS) documentés dans la littérature (Irwig et al., 2012).
Place du clascotérone dans le suivi après une greffe (perspective à l'étude)
Pour les patients ayant subi une greffe de cheveux par technique FUE ou Choi Pen, la prévention de la chute des cheveux non greffés (shock loss et progression de l'alopécie native) est un enjeu connu. Les recommandations ISHRS (2024) décrivent un suivi médical pluri-modal type, dans lequel un anti-androgène topique comme le clascotérone pourrait trouver sa place une fois autorisé. Le schéma ci-dessous est présenté à titre éducatif ; il ne décrit pas une offre de soins de Renaissance Clinique, qui ne prescrit pas ce médicament :
Cette approche multi-cible décrite dans la littérature — vasodilatation (minoxidil), inhibition de la 5α-réductase (finastéride, si toléré et prescrit) et, à terme, blocage local du récepteur AR (clascotérone, une fois disponible) — correspond aux principes énoncés par l'ISHRS (2024) pour limiter la progression de l'alopécie native après une greffe. Le choix et l'association éventuelle des molécules relèvent d'une prescription médicale individualisée par un dermatologue.
Statut réglementaire et disponibilité en France
Le clascotérone à 1 % (Winlevi) est approuvé par la FDA depuis août 2020 pour le traitement de l'acné et est disponible aux États-Unis (Cassiopea, prix US $700/mois en 2024). La concentration 7,5 % destinée à l'alopécie est en cours d'évaluation par la FDA et l'EMA. Selon Cosmo Pharmaceuticals (Investor Day 2024), la mise sur le marché européen est attendue entre 2027 et 2028, sous réserve de l'aboutissement des essais Phase III complémentaires en cours sur 1500+ patients.
À ce jour, le clascotérone n'est donc pas disponible comme traitement de l'alopécie en France : il n'a pas d'AMM dans cette indication et n'est pas remboursé par la Sécurité sociale. Toute question relative à un éventuel accès anticipé ou à une alternative relève strictement d'une consultation médicale auprès d'un dermatologue. Renaissance Clinique, en tant que clinique de greffe de cheveux, ne prescrit pas ce médicament et n'en organise pas la délivrance.
Femmes, grossesse et allaitement
Le clascotérone est particulièrement intéressant chez les femmes atteintes d'alopécie androgénétique féminine (FPHL), car le finastéride leur est contre-indiqué en âge de procréer (risque tératogène — féminisation des fœtus mâles). Le clascotérone, agissant localement sans passage systémique significatif, est a priori compatible avec une utilisation féminine.
Toutefois, selon la notice FDA Winlevi (2020), aucune étude formelle n'a été conduite chez la femme enceinte ou allaitante. Par principe de précaution, le clascotérone est déconseillé pendant la grossesse et l'allaitement en l'absence de données spécifiques. Les essais Phase III incluant des femmes pré-ménopausées sont en cours et publieront leurs résultats en 2026-2027.
Si vous êtes une femme atteinte d'alopécie androgénétique et envisagez le clascotérone : (1) consultez d'abord un dermatologue spécialisé en trichologie ; (2) bilan hormonal recommandé (testostérone, DHEA-S, SHBG, ferritine, TSH) ; (3) en cas de désir de grossesse, attendre la fin du désir de conception ou opter pour minoxidil seul.
Conclusion et perspectives
Le clascotérone représente une piste intéressante pour les patients qui cherchent une alternative au finastéride sans effets secondaires systémiques. Les données cliniques de Phase III sont encourageantes, mais la disponibilité en Europe pour l'alopécie n'est pas encore effective : tant que l'AMM n'est pas obtenue, il ne s'agit pas d'un traitement accessible en France pour cette indication.
Renaissance Clinique est spécialisée dans la greffe de cheveux et ne prescrit pas de traitement médicamenteux comme le clascotérone : pour toute question sur un traitement médical de l'alopécie, l'interlocuteur compétent est un dermatologue. Pour aller plus loin sur le plan informatif, consultez nos pages sur la comparaison avec le finastéride et sur les effets secondaires.
Les traitements médicaux comme celui-ci ralentissent la chute mais ne restaurent pas les zones dégarnies, et leur effet cesse à l'arrêt. Renaissance Clinique est spécialisée dans la greffe de cheveux (FUE et technique Choi Pen) : un résultat permanent en une seule intervention. Nos chirurgiens évaluent gratuitement votre cas.
Sources et références
- 1Piraccini et al. – JAAD 2024 (Phase III Breezula)Autorité
Étude Phase III sur 504 patients démontrant l'efficacité du clascotérone topique 7,5 % à 12 mois (+10,2 cheveux/cm² vs +1,6 placebo).
- 2ISHRS — Position on Topical Anti-Androgens (2024)Autorité
Recommandations de la Société Internationale de Restauration Capillaire concernant les anti-androgènes topiques en post-greffe (introduction M3+).
- 3Kaufman et al. – NEJM 1998 (Finasteride MAA Trial)Autorité
Étude pivotale sur 5 ans du finastéride 1 mg oral établissant le standard thérapeutique de référence (+30 % cheveux à 12 mois, 2-3 % effets secondaires sexuels).
- 4FDA — Winlevi (clascoterone 1%) Prescribing InformationAutorité
Notice officielle FDA — section Adverse Reactions et pharmacocinétique (demi-vie systémique < 5 min, métabolisation cortexolone).
- 5Cosmo Pharmaceuticals — Investor Day 2024
Communication officielle du calendrier réglementaire et résultats Phase III par le promoteur.
- 6HAS — Recommandations sur l'alopécie androgénétique (2023)Autorité
Recommandations françaises de référence sur la prise en charge de l'alopécie androgénétique (HAS, 2023).
- 7NCBI Bookshelf — Androgenetic Alopecia (StatPearls 2024)Autorité
Référence médicale ouverte sur l'alopécie androgénétique : épidémiologie (80 % hommes/40 % femmes post-ménopausées), physiopathologie et options thérapeutiques.
- 8Irwig et al. – J Sex Med 2012 (Post-Finasteride Syndrome)Autorité
Documentation des cas de post-finasteride syndrome (PFS) — base de la recherche d'alternatives sans effet systémique.
Questions fréquentes
Le clascotérone est-il disponible en France pour la calvitie ?
Non. La forme à 1 % (Winlevi, indiquée pour l'acné) est commercialisée aux États-Unis depuis 2020, mais la concentration à 7,5 % pour l'alopécie n'a pas d'AMM en France ni en Europe. Selon Cosmo Pharmaceuticals (2024), la mise sur le marché européen est attendue entre 2027 et 2028, sous réserve des essais en cours. Tant que l'autorisation n'est pas accordée, il n'est pas disponible comme traitement de la calvitie en France.
Quels sont les effets secondaires du clascotérone ?
Selon Piraccini et al. (JAAD 2024), les effets indésirables sont principalement locaux : irritation cutanée (5-8 %), sécheresse (3-5 %), prurit (2-3 %), érythème (1-2 %). Aucun effet systémique sur la libido, la fonction érectile ou les taux hormonaux n'a été observé dans les essais Phase III sur 504 patients à 12 mois.
Clascotérone ou finastéride : lequel choisir ?
Les deux molécules sont efficaces sur l'alopécie androgénétique. Le finastéride oral (Kaufman NEJM 1998) est plus puissant en valeur absolue mais peut entraîner des effets secondaires sexuels chez 2 à 3 % des patients. Le clascotérone topique (Piraccini JAAD 2024) offre un meilleur profil de tolérance systémique. Pour les patients intolérants au finastéride ou souhaitant éviter le risque hormonal, le clascotérone est l'alternative idéale.
Le clascotérone aura-t-il un intérêt après une greffe de cheveux ?
C'est l'une de ses indications théoriques les plus discutées : préserver les cheveux natifs et limiter la progression de l'alopécie autour de la zone greffée. Les recommandations ISHRS (2024) évoquent l'introduction d'un anti-androgène topique après cicatrisation complète (à partir du 3e mois environ). Cela reste toutefois conditionné à la disponibilité du produit, qui n'a pas encore d'AMM pour l'alopécie en France. Renaissance Clinique ne prescrit pas ce médicament ; toute prescription relève d'un dermatologue.
Combien coûtera le clascotérone et sera-t-il remboursé ?
Aucun prix officiel n'existe en France pour l'indication alopécie, puisque le produit n'y est pas commercialisé. À titre indicatif, aux États-Unis, le Winlevi 1 % (acné) coûte environ US $700/mois. Le remboursement éventuel par la Sécurité sociale ne pourra être déterminé qu'après l'obtention de l'AMM et la fixation d'un prix. Cette page ne fournit pas de filière d'approvisionnement : pour toute question, consultez un dermatologue.
Le clascotérone fonctionne-t-il chez la femme ?
Les études Phase II préliminaires (Cassiopea) sur 96 femmes pré-ménopausées atteintes d'alopécie androgénétique féminine (FPHL) montrent des résultats positifs en cours de publication. Le clascotérone est particulièrement intéressant pour les femmes car le finastéride leur est contre-indiqué en âge de procréer. Pendant grossesse et allaitement, il reste déconseillé par principe de précaution (manque de données).
Combien de temps avant de voir des résultats avec le clascotérone ?
Selon les données Phase III (Breezula 7,5 %), une amélioration cliniquement perceptible apparaît entre M3 et M6 chez la majorité des répondants. Le pic d'efficacité est observé entre M6 et M12. Un essai inférieur à 6 mois n'est pas concluant. L'arrêt du traitement entraîne une perte progressive de l'effet sur 6-12 mois.
Peut-on combiner clascotérone, minoxidil et finastéride ?
Sur le plan pharmacologique, ces molécules agissent à des niveaux différents de la cascade : minoxidil (vasodilatation), finastéride (5α-réductase systémique), clascotérone (récepteur AR local). La littérature (ISHRS 2024) décrit leur association possible pour les cas évolutifs ou réfractaires, sous suivi médical rapproché. Une telle association suppose toutefois que chaque molécule soit autorisée et prescrite par un médecin — ce qui n'est pas encore le cas du clascotérone en France.
Aller plus loin
FUE et Choi Pen — restauration permanente de la densité.
Forfaits tout compris — évaluation gratuite de votre cas.
Efficacité, profil de sécurité, coût et indications.
Tolérance locale, données systémiques, populations à risque.
Données et recommandations ISHRS sur l'usage post-greffe (information).
Le standard depuis 1997.
Vasodilatateur topique de référence.
Causes, évolution, options thérapeutiques.