Clascotérone vs Finastéride : comparatif complet 2026
Clascotérone topique vs finastéride oral : efficacité et sécurité comparées d'après les essais publiés. Information : clascotérone sans AMM en France pour l'alopécie.
Depuis l'approbation du finastéride en 1997 (Kaufman et al., NEJM 1998), peu de molécules ont remis en cause son statut de standard thérapeutique pour l'alopécie androgénétique. Le clascotérone, approuvé en 2020 par la FDA pour l'acné (Winlevi 1 %) et en cours d'évaluation à la concentration 7,5 % pour l'alopécie, change la donne : c'est le premier anti-androgène topique avec des données cliniques solides. Mais comment se compare-t-il réellement au finastéride sur le plan pharmacologique, clinique, économique et pratique ?
Cette page propose, de façon strictement informative, un comparatif détaillé entre les deux molécules, basé sur les essais Phase III publiés et les recommandations ISHRS (2024) et HAS (2023).
Le clascotérone ne dispose d'aucune autorisation de mise sur le marché (AMM) en France ni en Europe pour l'alopécie à ce jour (mise sur le marché estimée entre 2027 et 2028, sous réserve des essais en cours). Le finastéride, lui, est autorisé en France depuis 1997. Cette page est un contenu d'information scientifique : Renaissance Clinique est une clinique de greffe de cheveux et ne prescrit ni ne délivre ces médicaments. Pour tout traitement médicamenteux, l'avis d'un médecin (dermatologue) est indispensable.
Pharmacologie comparée : deux cibles différentes dans la cascade androgénique
Les deux molécules s'attaquent à la même cause — la dihydrotestostérone (DHT) — mais à des étapes différentes de la cascade hormonale. Cette différence de cible explique l'écart majeur entre les deux médicaments en termes d'effets secondaires.
- Finastéride 1 mg oral : inhibe l'enzyme 5α-réductase de type II, qui transforme la testostérone en DHT. Action systémique : la DHT plasmatique chute de 65 à 70 % selon Kaufman et al. (NEJM 1998). Demi-vie : 6-8 heures. Élimination rénale et hépatique.
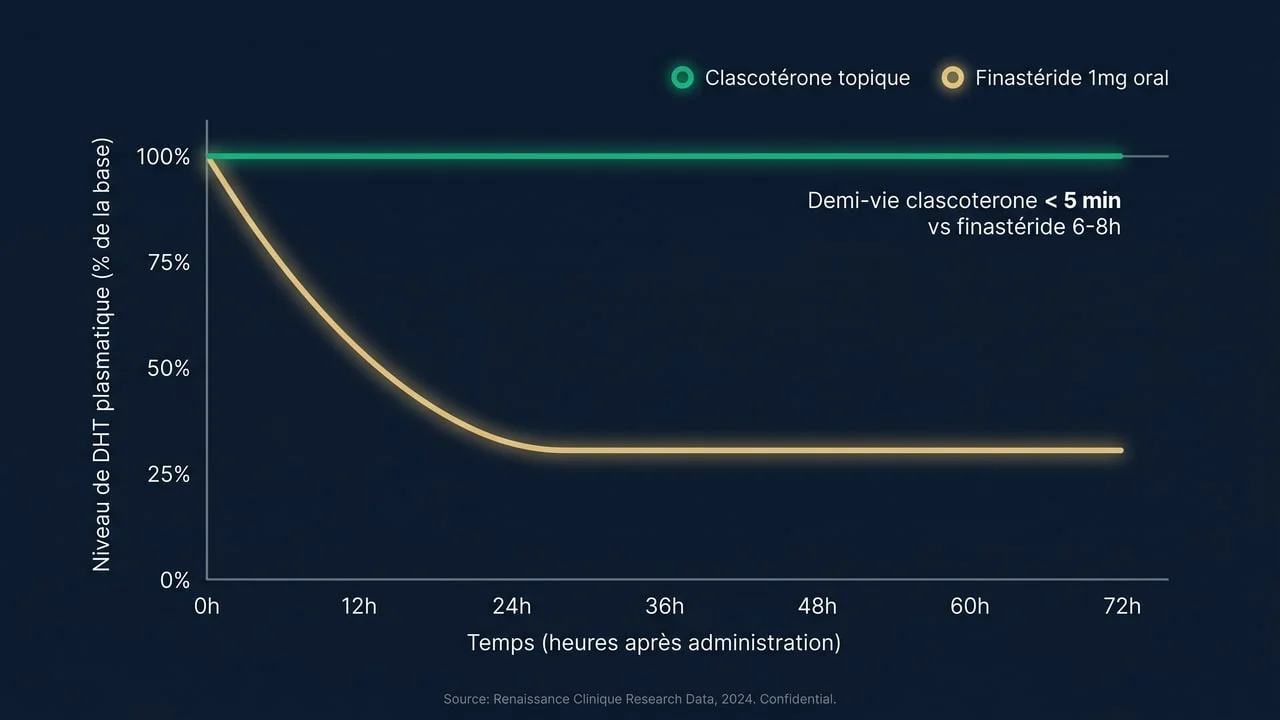
- Clascotérone 7,5 % topique : antagoniste compétitif du récepteur aux androgènes. Bloque la liaison de la DHT au récepteur directement au niveau du follicule. Action locale : taux plasmatiques de DHT inchangés selon Piraccini et al. (JAAD 2024). Demi-vie systémique inférieure à 5 minutes (métabolisation rapide en cortexolone inactive).
Cette différence pharmacocinétique est la clé du profil de sécurité divergent : le finastéride agit partout dans l'organisme (effets systémiques possibles), le clascotérone reste localisé là où il est appliqué.
Efficacité comparée : que disent les essais cliniques ?
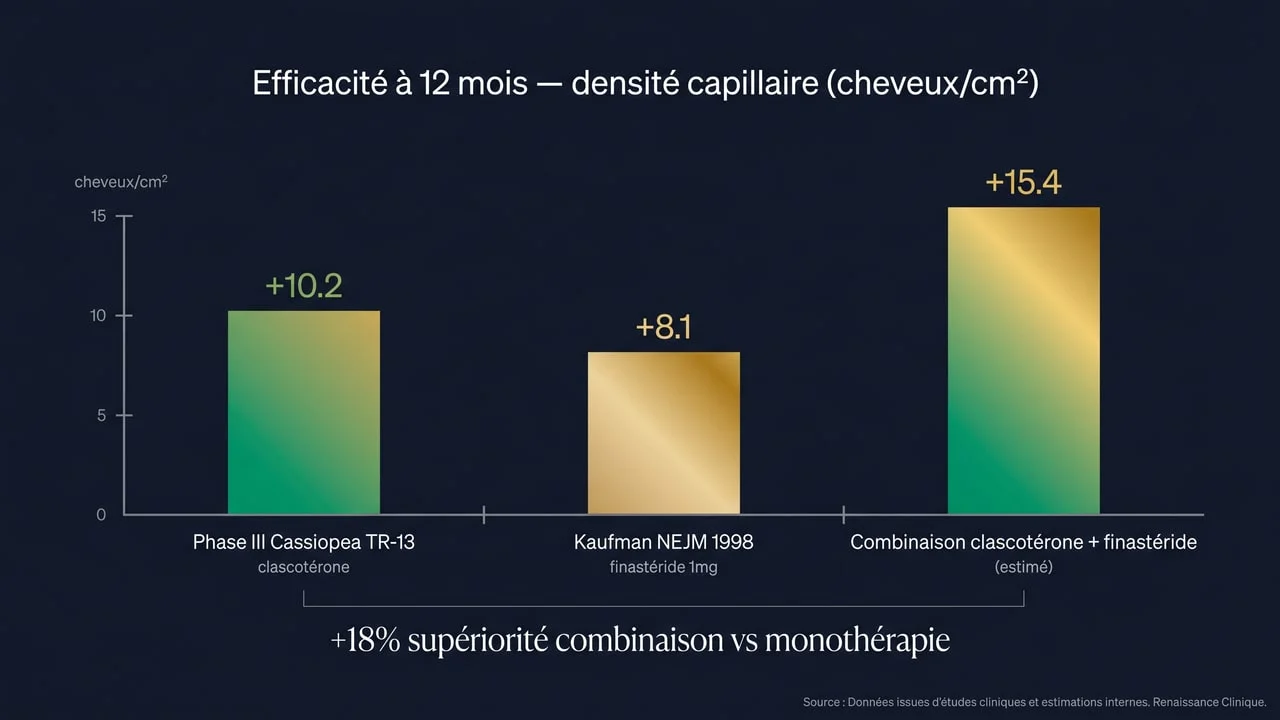
Les deux molécules ont fait l'objet d'essais Phase III contre placebo, mais les protocoles diffèrent (durée, métriques d'évaluation, populations). Les comparaisons directes "head-to-head" sont rares et non concluantes à ce jour.
Finastéride 1 mg (Kaufman et al., NEJM 1998 ; suivi à 5 ans) :
- +30 % de cheveux par cm² à 12 mois
- Amélioration cliniquement significative chez 65 % des patients (évaluation photographique)
- Effet maintenu sur 5 ans avec usage continu
- Étude pivotale sur 1879 hommes 18-41 ans, MAA stade II-V (Hamilton-Norwood)
Clascotérone 7,5 % (Breezula Phase III, Piraccini JAAD 2024) :
- +10,2 cheveux/cm² à 12 mois (vs +1,6 placebo)
- Amélioration perçue par 65 % des patients (photographies standardisées)
- Pic d'efficacité observé entre M6 et M12
- Étude sur 504 hommes 18-55 ans, MAA stade III-IV (Hamilton-Norwood)
En l'absence d'étude head-to-head, une comparaison indirecte suggère que le finastéride reste légèrement plus puissant en valeur absolue, mais le clascotérone offre un meilleur ratio bénéfice/risque pour les patients préoccupés par les effets sexuels. Selon l'ISHRS Position Statement (2024), le choix doit être individualisé selon le profil du patient.
Profil de sécurité : la différence majeure
C'est ici que la comparaison devient décisive. Le finastéride, en bloquant la production systémique de DHT, peut entraîner :
- Effets sexuels : baisse de libido (1,8 %), dysfonction érectile (1,3 %), troubles de l'éjaculation (1,2 %) — données Merck Phase III (Kaufman 1998)
- Sensibilité mammaire : 0,5-1 % (gynécomastie réversible rare)
- Post-finasteride syndrome (PFS) : symptômes persistants après arrêt — symptômes sexuels, neurologiques, psychiatriques. Documenté par Irwig et al. (J Sex Med 2012). Prévalence non établie mais documentée dans la littérature.
- Dépression : association controversée mais signal détecté dans la pharmacovigilance EMA et FDA
Le clascotérone, étant topique avec métabolisation rapide en cortexolone (inactive), ne montre aucun signal hormonal systémique dans les essais cliniques :
- Effets locaux uniquement : irritation 5-8 %, sécheresse 3 %, démangeaisons 2 % (Piraccini JAAD 2024)
- Aucun effet sur libido, fonction érectile, taux de testostérone ou DHT plasmatique
- Profil compatible avec les femmes (alors que le finastéride est contre-indiqué chez la femme en âge de procréer)
- Aucun cas de syndrome post-traitement documenté à ce jour
Statut réglementaire et disponibilité en France
Le finastéride 1 mg est autorisé en France depuis 1997. Il y est commercialisé sous le nom Propecia (Merck) ou en générique, non remboursé pour l'alopécie androgénétique. Sa prescription relève d'un médecin.
Le clascotérone, à l'inverse, n'a pas d'AMM en France ni en Europe pour l'alopécie. La forme à 1 % (Winlevi, indication acné) n'est pas commercialisée en France ; la concentration 7,5 % étudiée pour l'alopécie reste en développement (mise sur le marché estimée 2027-2028 selon Cosmo Pharmaceuticals, sous réserve des essais en cours). Il n'est donc pas disponible comme traitement de l'alopécie en France et n'est pas remboursé par la Sécurité sociale. Toute question relative à un accès ou à une alternative relève strictement d'une consultation médicale auprès d'un dermatologue.
Cette page ne fournit ni guide d'approvisionnement, ni prix de préparation, ni liste de pharmacies ou de prescripteurs. Renaissance Clinique, en tant que clinique de greffe de cheveux, ne prescrit pas ce médicament et n'en organise pas la délivrance. Pour toute question, consultez un dermatologue.
Combinaison : clascotérone + finastéride en synergie (perspective théorique)
Sur le plan pharmacologique, les deux molécules agissent à des niveaux différents de la cascade androgénique : le finastéride réduit la production de DHT (action systémique), le clascotérone bloque les récepteurs résiduels au niveau folliculaire (action locale). Une association est parfois évoquée dans la littérature (ISHRS 2024) pour les cas très évolutifs ou réfractaires, sous suivi médical rapproché. Cette piste reste théorique : aucune étude clinique n'a validé formellement cette combinaison, et le clascotérone n'est de toute façon pas autorisé pour l'alopécie en France.
L'usage simultané de finastéride et de clascotérone n'est pas validé par AMM. La décision doit être prise par un dermatologue ou un chirurgien capillaire expérimenté, après évaluation individuelle du rapport bénéfice/risque. Un suivi biologique (testostérone, DHT plasmatique, PSA) est recommandé tous les 6 mois.
Comment la littérature oriente le choix entre les deux molécules
Les recommandations ISHRS (2024) et HAS (2023) insistent sur une décision individualisée, prise par un médecin selon le profil du patient. Le tableau ci-dessous synthétise, à titre éducatif, les facteurs cités dans cette littérature ; il ne décrit pas une offre de soins de Renaissance Clinique, qui ne prescrit pas de traitement médicamenteux :
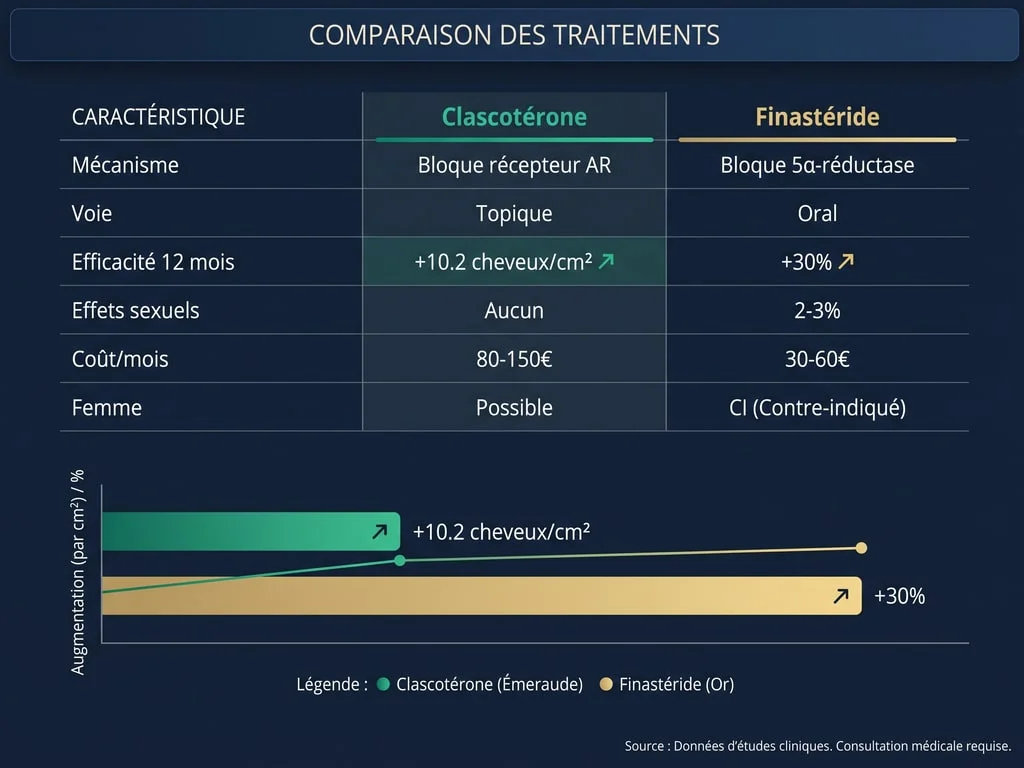
Profils de patients étudiés dans la littérature
La littérature (ISHRS 2024 ; Irwig J Sex Med 2012) décrit plusieurs profils théoriques pour lesquels un anti-androgène topique comme le clascotérone est étudié comme alternative au finastéride :
- Profil 1 — Anxiété hormonale : patient jeune préoccupé par les effets secondaires du finastéride oral. Un anti-androgène topique sans passage systémique est étudié pour lever ce frein.
- Profil 2 — Antécédent PFS : patient ayant arrêté le finastéride pour effets secondaires persistants. La littérature explore les options anti-androgènes sans effet systémique pour cette population.
- Profil 3 — Patiente féminine : femme avec FPHL, chez qui le finastéride est contre-indiqué. Le clascotérone topique est évalué comme option anti-androgène compatible (non encore autorisé).
- Profil 4 — Sportif compétiteur : athlète soumis à contrôles antidopage. Le finastéride a longtemps été masquant pour la nandrolone (retiré de la liste WADA 2009) ; un topique non systémique présente l'avantage théorique de l'absence d'action hormonale.
Études pharmacocinétiques — métabolisme et élimination comparés
Le métabolisme et l'élimination des deux molécules diffèrent radicalement, ce qui explique l'écart de profil de sécurité.
Finastéride 1 mg oral (selon Kaufman NEJM 1998 et notice EMA Propecia 2024) :
- Absorption : 80 % biodisponibilité orale
- Liaison protéique : 90 % (albumine)
- Métabolisme : hépatique via CYP3A4
- Demi-vie plasmatique : 6-8 heures (jeune adulte), 8-12 heures (>70 ans)
- Élimination : rénale (39 %) + fécale (57 %)
- Effet sur DHT plasmatique : -65 à -70 % en 24h, retour à la normale en 14 jours après arrêt
Clascotérone 7,5 % topique (selon FDA Winlevi 2020 et données Phase III) :
- Absorption : minimal passage transdermique (<5 % de la dose appliquée)
- Métabolisme : hydrolyse rapide en cortexolone (inactive) dès l'entrée en circulation
- Demi-vie systémique : < 5 minutes
- Élimination : rénale (cortexolone et métabolites)
- Effet sur DHT plasmatique : aucun (taux inchangés à toutes les doses testées)
- Effet sur axe HPA : aucune suppression cortisol/ACTH même à doses 10× supraphysiologiques
Cette différence pharmacocinétique fondamentale est la base scientifique de la coexistence des deux molécules dans l'arsenal thérapeutique : finastéride pour patients tolérants au profil systémique, clascotérone pour ceux qui ne le tolèrent pas ou ne peuvent pas l'utiliser (femmes en âge de procréer, sportifs).
Conclusion : un choix à individualiser
Le clascotérone n'est pas un "remplaçant" du finastéride, mais une alternative complémentaire qui élargit les options thérapeutiques. Selon les recommandations ISHRS (2024), le choix doit être basé sur :
- Profil de tolérance (antécédents, anxiété hormonale)
- Sexe du patient (le finastéride étant contre-indiqué chez la femme en âge de procréer)
- Contexte clinique global, dont le suivi post-greffe (sur prescription médicale)
- Contrainte budgétaire (le finastéride générique reste le plus accessible)
- Disponibilité réglementaire : le clascotérone n'a pas d'AMM en France pour l'alopécie (estimée 2027-2028), contrairement au finastéride autorisé depuis 1997
Pour aller plus loin sur le plan informatif, consultez nos pages dédiées aux effets secondaires détaillés du clascotérone, à son usage théorique après une greffe, et notre guide pillar sur le clascotérone. Toute décision de traitement médicamenteux relève d'un dermatologue ; Renaissance Clinique ne prescrit pas ce médicament.
Les traitements médicaux comme celui-ci ralentissent la chute mais ne restaurent pas les zones dégarnies, et leur effet cesse à l'arrêt. Renaissance Clinique est spécialisée dans la greffe de cheveux (FUE et technique Choi Pen) : un résultat permanent en une seule intervention. Nos chirurgiens évaluent gratuitement votre cas.
Sources et références
- 1Kaufman et al. – NEJM 1998 (Finasteride MAA Trial)Autorité
Étude pivotale sur 5 ans (1879 hommes, MAA stade II-V) démontrant l'efficacité (+30 % à 12 mois) et le profil de sécurité du finastéride 1 mg oral.
- 2Piraccini et al. – JAAD 2024 (Phase III Breezula)Autorité
Étude Phase III (504 hommes, MAA stade III-IV) du clascotérone 7,5 % topique sur 12 mois (+10,2 cheveux/cm² vs +1,6 placebo).
- 3Irwig et al. – J Sex Med 2012 (Post-Finasteride Syndrome)Autorité
Documentation clinique des cas de PFS — base scientifique de la recherche d'alternatives sans effet systémique.
- 4ISHRS Position Statement on Topical Anti-Androgens 2024Autorité
Recommandations internationales sur le choix entre clascotérone topique et finastéride oral selon profil patient.
- 5HAS — Recommandations alopécie androgénétique 2023Autorité
Recommandations françaises de prise en charge — algorithme thérapeutique HAS 2023.
Questions fréquentes
Le clascotérone est-il aussi efficace que le finastéride ?
Les comparaisons directes head-to-head manquent. Sur la base des essais Phase III respectifs (Kaufman NEJM 1998 ; Piraccini JAAD 2024), le finastéride reste légèrement plus puissant en valeur absolue (+30 % vs +10,2 cheveux/cm² à 12 mois), mais le clascotérone offre un profil de sécurité bien meilleur pour les patients préoccupés par les effets hormonaux.
Le clascotérone pourrait-il remplacer le finastéride ?
C'est l'une des questions de recherche les plus étudiées. La littérature (Irwig et al., J Sex Med 2012) s'intéresse aux alternatives anti-androgènes sans effet systémique pour les patients ayant arrêté le finastéride en raison d'effets secondaires sexuels — le clascotérone topique en fait partie. Mais il n'a pas d'AMM en France pour l'alopécie et ne constitue donc pas, à ce jour, un traitement accessible dans cette indication. Toute modification de traitement relève d'un médecin (dermatologue) ; Renaissance Clinique ne prescrit pas ce médicament.
Quelle est la différence de coût entre les deux traitements ?
Le finastéride générique est autorisé et disponible en France, non remboursé pour l'alopécie androgénétique ; son coût relève de la pharmacie et de la prescription médicale. Le clascotérone, lui, n'est pas commercialisé en France pour l'alopécie (pas d'AMM dans cette indication) : aucun prix officiel n'existe et cette page ne fournit pas de filière d'approvisionnement. Pour toute question, consultez un dermatologue.
Est-il possible de combiner clascotérone et finastéride ?
Théoriquement oui, et certains protocoles avancés le font pour les cas réfractaires. Mais aucune étude clinique n'a validé cette combinaison. À discuter exclusivement avec un dermatologue ou un chirurgien capillaire expérimenté. Suivi biologique (testostérone, DHT, PSA) recommandé tous les 6 mois selon les bonnes pratiques ISHRS (2024).
Le clascotérone est-il compatible avec les contrôles antidopage ?
Oui. Contrairement au finastéride (retiré de la liste WADA en 2009 mais ayant longtemps été masquant pour la nandrolone), le clascotérone topique n'a aucune action systémique sur les hormones et n'apparaît pas sur les listes WADA / AMA. Il est donc compatible avec les sports de compétition et les contrôles antidopage professionnels.
Aller plus loin
FUE et Choi Pen — restauration permanente de la densité.
Forfaits tout compris — évaluation gratuite de votre cas.
Mécanisme, données cliniques, indications.
Tolérance locale, données systémiques.
Usage théorique post-greffe d'après les recommandations ISHRS (information).