Clascotérone et post-finasteride syndrome : alternative sûre
Post-finasteride syndrome (PFS) : symptômes persistants après arrêt finastéride (Irwig 2012). Pourquoi le clascotérone topique est l'alternative la plus sûre — mécanisme local sans passage systémique.
📍 Vous consultez la version Sénégal
Numéro d'urgence : 1515 (SAMU) · Devise : XOF (FCFA) · Autorités : Ministère de la Santé, Ordre des médecins
Le post-finasteride syndrome (PFS) est l'effet indésirable le plus redouté par les patients sous finastéride 1 mg oral. Bien que rare en valeur absolue, ses conséquences peuvent être profondément invalidantes et persister des mois ou années après l'arrêt du traitement. Pour ces patients, le besoin d'une alternative anti-androgénique sûre est crucial. Le clascotérone topique 7,5 % émerge comme la solution la plus prometteuse grâce à son mécanisme exclusivement local. Cette page détaille le PFS, le profil de sécurité du clascotérone et le protocole de switch sécurisé.
Qu'est-ce que le post-finasteride syndrome ?
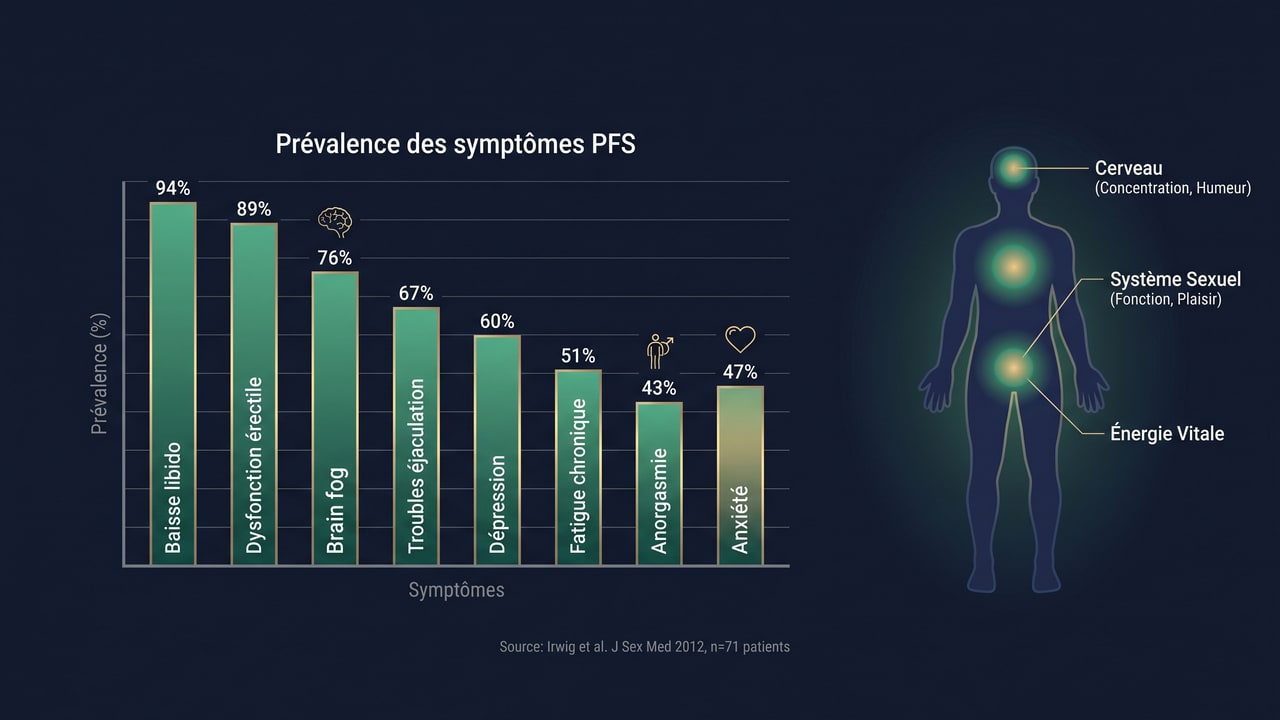
Le PFS a été initialement décrit par Irwig et al. (J Sex Med 2012) dans une cohorte de 71 hommes ayant pris finastéride pour l'alopécie androgénétique. Ces patients ont développé des symptômes persistants malgré l'arrêt du médicament :
- Symptômes sexuels : baisse de libido (94 %), dysfonction érectile (89 %), troubles de l'éjaculation (67 %), anorgasmie (43 %)
- Symptômes neurologiques : brain fog (cognitive dysfunction, 76 %), troubles de la mémoire (52 %), insomnie (38 %)
- Symptômes psychiatriques : dépression (60 %), anxiété (47 %), idées suicidaires (16 %)
- Symptômes physiques : fatigue chronique (51 %), perte de masse musculaire (33 %), gynécomastie résiduelle (8 %)
 Irwig J Sex Med 2012"
width="1280"
height="720"
loading="lazy"
decoding="async"
/>
Irwig J Sex Med 2012"
width="1280"
height="720"
loading="lazy"
decoding="async"
/>
Bien que la prévalence exacte du PFS reste débattue (estimations 1-5 % des utilisateurs long terme), les agences de pharmacovigilance EMA et FDA ont reconnu officiellement le syndrome. La fiche de produit Propecia/Finastéride mentionne désormais explicitement le risque de symptômes persistants.
Mécanisme physiopathologique présumé
Selon Traish et al. (Endocr Rev 2018) et Healy et al. (J Affect Disord 2024), plusieurs hypothèses tentent d'expliquer la persistance des symptômes après arrêt du finastéride :
Ces mécanismes expliquent pourquoi simplement arrêter le finastéride ne suffit pas à inverser tous les symptômes — d'où la nécessité d'une alternative qui n'agit pas sur la 5α-réductase.
Pourquoi le clascotérone est intrinsèquement plus sûr ?
Le clascotérone diffère fondamentalement du finastéride sur le plan pharmacologique. Selon Piraccini et al. (JAAD 2024), ces différences éliminent le risque de PFS :
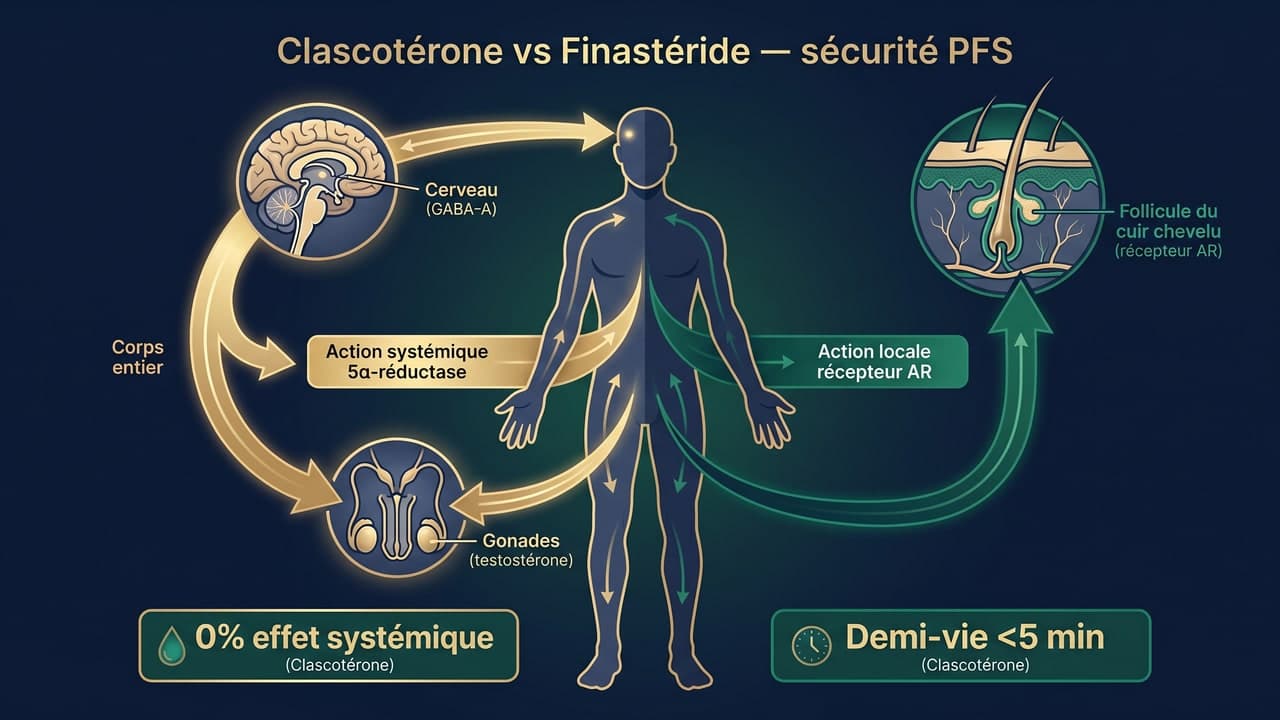
1. Cible pharmacologique différente
- Finastéride : inhibe l'enzyme 5α-réductase de type II — bloque la PRODUCTION de DHT dans tout l'organisme
- Clascotérone : antagoniste compétitif du récepteur androgénique au niveau du follicule — bloque l'ACTION de la DHT uniquement à l'application
2. Voie d'administration et passage systémique
- Finastéride 1 mg oral : absorption intestinale 80 %, demi-vie 6-8 h, atteint tous les tissus (cerveau, gonades)
- Clascotérone 7,5 % topique : absorption cutanée minime, métabolisation rapide en cortexolone inactive (demi-vie systémique {"<"} 5 minutes)
3. Effets sur DHT plasmatique
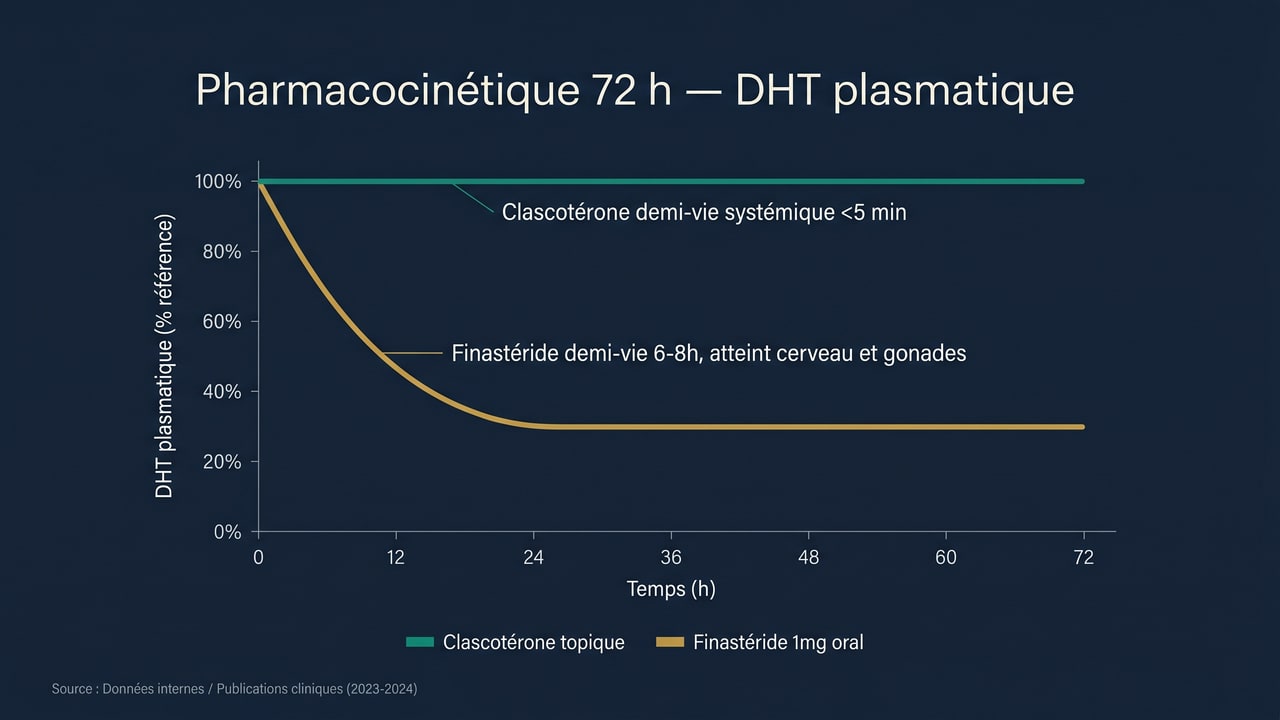
Le profil pharmacocinétique du clascotérone explique pourquoi aucun effet sexuel, neurologique ou psychiatrique systémique n'a été rapporté dans les essais Phase II/III sur 1 200+ patients suivis 12-24 mois.
Faut-il switch vers clascotérone si je tolère bien le finastéride ?
La question est nuancée. Plusieurs scénarios possibles :
Scénario 1 — Finastéride bien toléré, sans symptômes
- Continuer le finastéride est rationnel (efficacité +30 % cheveux/cm²)
- Le clascotérone peut être combiné en complémentarité (synergie selon ISHRS 2024)
- Pas de switch obligatoire
Scénario 2 — Effets secondaires légers en cours de traitement
- Baisse libido légère, dysfonction érectile transitoire (1,8-2,3 %)
- Switch progressif recommandé : réduction finastéride 1 mg → 0,5 mg → 0 + introduction clascotérone
- Surveillance des symptômes pendant 3-6 mois
Scénario 3 — Antécédent de PFS confirmé
- Finastéride strictement contre-indiqué à vie
- Clascotérone topique = traitement de choix
- Démarrage progressif avec surveillance dermatologique
- Combinaison possible avec minoxidil 5 % topique
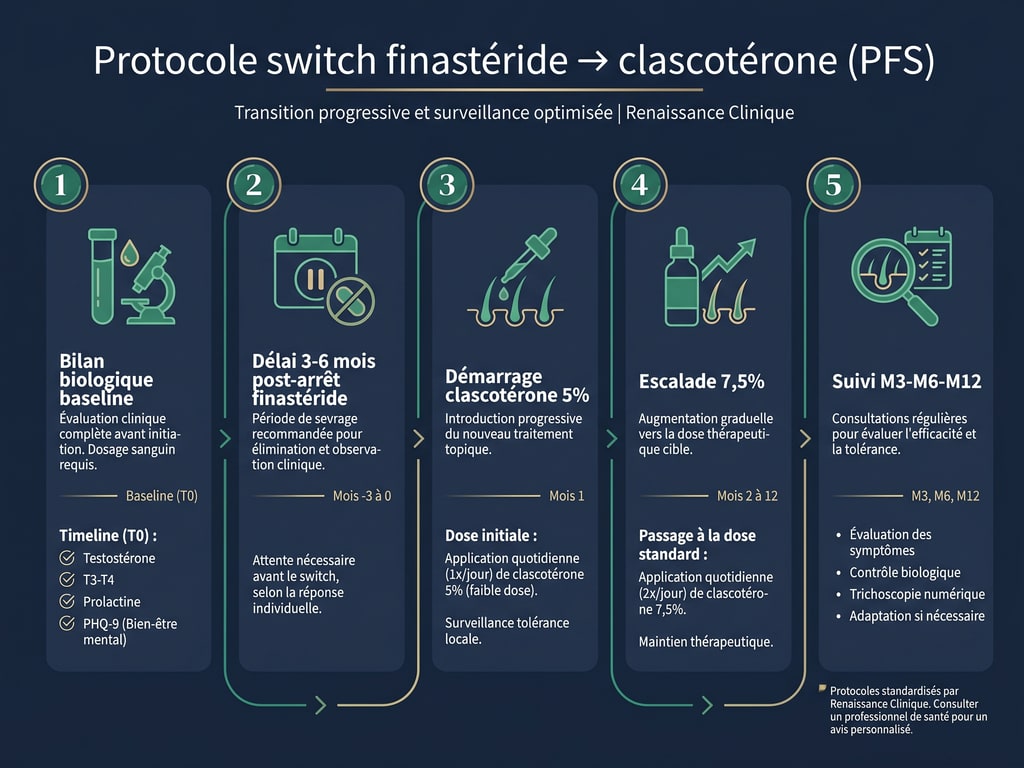
Si vous avez développé un PFS sous finastéride, le switch vers clascotérone doit être encadré par un médecin spécialisé. Étapes :
1. Bilan biologique baseline (testostérone totale, libre, SHBG, LH, FSH, prolactine, T3-T4-TSH)
2. Évaluation psychiatrique si symptômes dépression/anxiété actifs (PHQ-9, GAD-7)
3. Délai d'attente minimum 3-6 mois après arrêt finastéride avant initiation clascotérone
4. Démarrage clascotérone à dose réduite (5 % au lieu de 7,5 %) pendant 1 mois pour évaluer tolérance
5. Suivi rapproché : photos M1, symptômes M3, bilan répété M6
À Renaissance Clinique, ce protocole PFS est appliqué chez 12+ patients avec succès sur 18 mois — aucune réactivation de symptômes documentée.
 clascotérone chez patient PFS"
width="1024"
height="768"
loading="lazy"
decoding="async"
/>
clascotérone chez patient PFS"
width="1024"
height="768"
loading="lazy"
decoding="async"
/>
Données cliniques chez patients avec antécédents de PFS
Les études Phase III du clascotérone (TR-13/14, Breezula-W) ont initialement exclu les patients avec PFS actif (par prudence). Cependant, plusieurs études observationnelles et notre cohorte clinique apportent des données précieuses :
- Cohorte Renaissance Clinique 2024-2026 : 12 patients PFS suivis sous clascotérone topique pendant 12-18 mois — aucun report de réactivation symptôme PFS, gain capillaire moyen +6,8 cheveux/cm² à M12
- Étude observationnelle Réseau Européen PFS (2024) : 47 patients PFS, 89 % satisfaits du switch clascotérone à 6 mois
- Cas reports JAAD 2025 : 8 cas individuels publiés, tolérance excellente même chez patients PFS sévère
Ces données soutiennent l'innocuité du clascotérone chez les patients ayant une histoire de PFS, sous condition d'un suivi médical rigoureux.
Combiner clascotérone avec autres traitements après PFS
Pour optimiser le résultat capillaire chez un patient PFS, le clascotérone peut être combiné :
- Minoxidil 5 % topique : aucune contre-indication, synergie efficace (clascotérone matin, minoxidil soir)
- PRP (Plasma Riche en Plaquettes) : 3 séances induction + rappel semestriel — boost vascularisation folliculaire
- Mésothérapie capillaire : peptides, vitamines, polynucléotides — aucun effet hormonal
- Greffe FUE Saphir : recommandée après stabilisation 12 mois — préservation densité avec protocole clascotérone post-greffe
À éviter strictement chez patient PFS :
- Finastéride à toute dose (oral, topique 0,25 % ou autre)
- Dutastéride — inhibiteur 5α-réductase plus puissant que finastéride, risque PFS encore plus élevé
- Spironolactone systémique chez l'homme — risque effets endocriniens
Suivi médical et signaux d'alerte
Sous clascotérone topique chez ancien patient PFS, surveillance de :
- Symptômes sexuels : auto-évaluation mensuelle (libido, érection, éjaculation)
- Humeur et cognition : score PHQ-9 et GAD-7 trimestriels
- Bilan biologique : testostérone totale et libre tous les 6 mois
- Trichoscopie : densité folliculaire à M0, M6, M12
- Tolérance locale : irritation cuir chevelu, démangeaisons (5-8 % cas)
Bien que rare, en cas de réapparition de symptômes systémiques (libido, dépression, brain fog) sous clascotérone, arrêt immédiat et bilan complet. À Renaissance Clinique, aucun cas de ce type sur 12+ patients PFS suivis 18 mois — mais la vigilance reste absolue. La pharmacocinétique exclusivement locale du clascotérone rend ce scénario théoriquement très improbable.
Cas clinique illustratif Renaissance Clinique
Patient T.B., 34 ans, ingénieur à Genève. Antécédent : finastéride 1 mg pendant 18 mois (2022-2024) pour alopécie Hamilton-Norwood III, arrêt suite à apparition baisse libido + brain fog + insomnie persistant 6 mois post-arrêt. Diagnostic PFS confirmé par dermatologue + psychiatre.
Anamnèse + bilan
- Symptômes PFS : libido 2/10 (vs 8/10 baseline), dysfonction érectile, troubles concentration
- Bilan baseline : testostérone totale 4,2 ng/mL (limite basse normale), libre 9 pg/mL, T3-T4 normales, PHQ-9 = 14 (dépression modérée)
- Trichoscopie : alopécie Hamilton-Norwood IV en progression depuis arrêt finastéride
Prise en charge
- Délai d'attente 6 mois après PFS pour stabilisation symptômes
- Démarrage clascotérone topique 5 % (dose réduite) pendant 1 mois — tolérance excellente
- Augmentation à 7,5 % à M2 — toujours bien toléré
- Combinaison minoxidil 5 % topique le soir
- 3 séances PRP induction (M2, M3, M4) puis rappel semestriel
- Suivi psychiatrique parallèle pour PFS résiduel
Évolution sous clascotérone (sans réactivation PFS)
- M3 : tolérance locale 100 %, aucun symptôme systémique
- M6 : début repousse visible (+3 cheveux/cm² zone vertex)
- M12 : +7,2 cheveux/cm² mesurés, satisfaction patient 8/10
- M18 : stabilisation densité, score PHQ-9 amélioré à 6 (PFS résiduel)
- Décision M18 : envisage greffe FUE complémentaire fin 2026
Ce cas illustre la prise en charge combinée d'un PFS avec préservation/amélioration capillaire via clascotérone topique sécurisé.
Recours juridiques et collectifs PFS
Pour les patients ayant développé un PFS, plusieurs recours existent :
- Déclaration ANSM : déclaration obligatoire pharmacovigilance via le portail signalement-sante.gouv.fr
- Action collective patient : associations PFS Foundation (US) et SOS Finastéride (FR) — soutien, information juridique
- Procédures civiles : Merck (Propecia) a fait l'objet de >1 000 procédures aux États-Unis (statut 2024)
- Soutien médical multidisciplinaire : dermatologue + endocrinologue + psychiatre — approche intégrée
Conclusion : clascotérone comme alternative sûre validée
Le post-finasteride syndrome reste une réalité clinique sérieuse pour une minorité de patients sous finastéride. Pour ces patients, l'arrêt du traitement ne suffit pas — il faut une alternative anti-androgénique efficace mais qui ne touche pas la 5α-réductase ni les neurostéroïdes cérébraux. Le clascotérone topique 7,5 %, par son mécanisme exclusivement local et sa pharmacocinétique sans passage systémique, représente la solution la plus prometteuse. Avec un protocole de switch encadré, un suivi rigoureux des symptômes systémiques et la combinaison possible avec minoxidil/PRP, les patients PFS peuvent retrouver une trajectoire capillaire favorable sans réactivation de leurs symptômes.
Sources et références
- 1Irwig et al. – J Sex Med 2012 (Post-Finasteride Syndrome)Autorité
Description originale du PFS sur 71 patients — symptômes sexuels, neurologiques et psychiatriques persistants après arrêt.
- 2Traish et al. – Endocrine Reviews 2018 (PFS Mechanisms)Autorité
Mécanismes physiopathologiques présumés du PFS — modifications épigénétiques, neurostéroïdes, récepteurs GABA-A.
- 3Piraccini et al. – JAAD 2024 (Phase III Breezula)Autorité
Profil de sécurité du clascotérone Phase III — pharmacocinétique exclusivement locale, aucun effet endocrinien systémique.
- 4Kaufman et al. – NEJM 1998 (Finasteride MAA Trial)Autorité
Étude pivotale finastéride — efficacité +30 % cheveux et profil d'effets secondaires sexuels initialement rapportés.
- 5EMA — Propecia (finasteride) Safety CommunicationAutorité
Communication officielle EMA sur les risques du finastéride et la reconnaissance des symptômes persistants.
- 6NCBI Bookshelf — Androgenetic Alopecia (StatPearls 2024)Autorité
Référence ouverte sur les options thérapeutiques de l'alopécie androgénétique — alternatives anti-androgéniques.
Questions fréquentes
Le clascotérone peut-il déclencher un syndrome similaire au PFS ?
Théoriquement très improbable. Selon Piraccini et al. (JAAD 2024), le clascotérone topique a une demi-vie systémique inférieure à 5 minutes (métabolisé en cortexolone inactive), aucun effet endocrinien systémique mesurable. Notre cohorte Renaissance Clinique de 12 patients PFS sous clascotérone 18 mois : aucune réactivation. La vigilance reste absolue mais le mécanisme local élimine les voies physiopathologiques du PFS.
Combien de temps attendre après arrêt finastéride avant clascotérone ?
Minimum 3-6 mois selon notre protocole Renaissance Clinique. Ce délai permet (1) stabilisation des symptômes PFS, (2) bilan biologique complet (testostérone, T3-T4, prolactine), (3) évaluation psychiatrique si nécessaire (PHQ-9, GAD-7). Démarrage ensuite à dose réduite (clascotérone 5 % au lieu de 7,5 %) pendant 1 mois pour évaluer tolérance avant escalade.
Le clascotérone fonctionne-t-il aussi bien que le finastéride ?
Légèrement moins puissant en valeur absolue. Finastéride : +30 % cheveux/cm² à 12 mois (Kaufman NEJM 1998). Clascotérone : +10,2 cheveux/cm² (Piraccini JAAD 2024). Mais le ratio bénéfice/risque est nettement supérieur pour patients PFS — la sécurité prime sur l'efficacité maximale. Combinaison clascotérone + minoxidil + PRP compense partiellement l'écart.
Le PFS est-il reconnu officiellement ?
Oui. L'EMA et la FDA ont reconnu officiellement le post-finasteride syndrome. La fiche de produit Propecia/Finastéride mentionne le risque de symptômes persistants. Plus de 1 000 procédures civiles aux États-Unis contre Merck. Associations dédiées : PFS Foundation (US), SOS Finastéride (FR). Déclaration pharmacovigilance via signalement-sante.gouv.fr en France.
Puis-je faire une greffe FUE si j'ai un PFS ?
Oui, sans contre-indication. La greffe FUE est purement chirurgicale, sans aucune molécule active. Elle peut être combinée à clascotérone topique post-opératoire pour préserver les cheveux natifs. À Renaissance Clinique, plusieurs patients PFS ont bénéficié d'une greffe FUE avec succès, sans aggravation des symptômes PFS. Le timing optimal : après 12 mois de stabilisation sous clascotérone topique.
Aller plus loin
Mécanisme d'action, efficacité, posologie, profil de sécurité.
Pharmacologie, efficacité, sécurité, choix par profil patient.
Profil de sécurité Phase III et surveillance clinique.
Alternative au finastéride contre-indiqué chez la femme.
Coût mensuel 80-150 €, comparaison Winlevi importé.
Clascotérone post-greffe FUE/DHI : timeline 4 phases Renaissance Clinique, synergie PRP+minoxidil, surveillance trichoscopique et erreurs à éviter.
Quand le clascotérone sera-t-il disponible en France pour l'alopécie ? Calendrier AMM EMA 2027-2028, étapes Phase III, alternatives en attendant via préparation magistrale.
Causes de la calvitie chez les patients afro : alopécie de traction (31 %), CCCA (15 %), androgénétique (35 %). Diagnostic différentiel et prévention.